近年、大気汚染防止の観点から、工場や発電所などから排出される排ガス中の硫黄酸化物(SOx)を除去する排煙脱硫技術がますます重要になっています。その中でも、水酸化マグネシウムスラリー吸収法は、高い脱硫効率と比較的扱いやすいという特徴から広く採用されています。この記事では、排煙脱硫の基本から水酸化マグネシウム法の詳細まで、初心者の方でも理解できるよう丁寧に解説していきます。
排煙脱硫とは
排煙脱硫とは、工場や発電所などの燃焼施設から排出される排ガス中に含まれる硫黄酸化物(SOx)を除去する技術です。SOxは大気汚染の原因物質の一つであり、酸性雨や呼吸器疾患などの健康被害を引き起こす可能性があります。そのため、排煙脱硫は環境保全と人々の健康を守るために不可欠な技術と言えます。
プロセス概要
水酸化マグネシウム法は、排煙脱硫方法の一つで、水酸化マグネシウム(Mg(OH)2)のスラリー(液体と固体の混合物)を吸収剤として使用します。排ガス中のSOxは、水酸化マグネシウムと反応して硫酸マグネシウム(MgSO4)などの物質に変換され、排ガスから除去され、廃水として放流されます。プロセスは主に以下3つの工程で構成されています。
吸収工程: SOxと水酸化マグネシウムの反応
酸化工程: 亜硫酸マグネシウムの硫酸マグネシウムへの酸化
回収工程: 硫酸マグネシウムの回収・処理
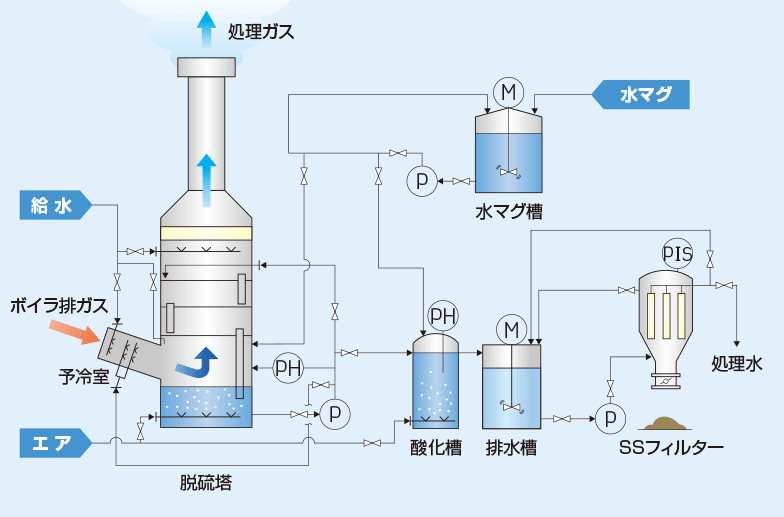
吸収工程
吸収工程では、排ガスを吸収塔に導入し、水酸化マグネシウムスラリーと接触させます。排ガス中の二酸化硫黄(SO2)は、水酸化マグネシウムと反応して以下のような反応が起きます。
SO2 + H2O → H2SO3
H2SO3 + Mg(OH)2 → MgSO3 + 2H2O
MgSO3 + H2SO3 → Mg(HSO3)2
また、吸収塔下部で空気酸化を行なう場合、以下の反応が起きます。
Mg(HSO3)2 + Mg(OH)2 → 2MgSO3 + 2H2O
MgSO3 + 1/2O2 → MgSO4
酸化工程
吸収工程から取り出されたスラリーには、亜硫酸水素マグネシウム(Mg(HSO3)2)や、亜硫酸マグネシウム(MgSO3)が残存します。これをそのまま水域に放流すると化学的酸素消費量(COD)を増大させてしまうため、酸化槽で空気を使用し、硫酸マグネシウムとします。酸化反応により生成した硫酸マグネシウムは無害なため環境へ放流されます。
Mg(HSO3)2 + O2 → MgSO4 + H2SO4
MgSO3 + 1/2O2 → MgSO4
メリット・デメリット
水酸化マグネシウムスラリー法のメリット・デメリットを以下にまとめます。
メリット
・システムが簡単であり、設備費は石灰スラリー吸収法に比べ安価
・スラリーは弱アルカリ性ではあるものの、毒性、腐食性がほとんどなく取り扱いが容易
・反応で生成する塩類の溶解度が大きく、スケーリングの心配がなく維持管理が容易
デメリット
・水酸化マグネシウムが石灰石よりも効果で運転費が高くなる
よく比較される石灰スラリー吸収法に関する記事もありますので、こちらも読んでもらえるとより理解が深まると思います。
最後に
現在主流になっている排煙脱硫プロセスについて、概要を紹介しました。役に立てば幸いです。
ご安全に!




コメント